آزمایشگاه ژئوشیمی
آشنایی با طیفسنجی جذب اتمی:
طیفسنجی جذب اتمی (AAS) یک روش اسپکتروسکوپی برای اندازهگیری کمی عناصر شیمیایی با استفاده از جذب اشعه نوری (نور) توسط اتم در حالت گازی است. در شیمی تجزیه این تکنیک برای تعیین غلظت یک عنصر خاص در یک نمونه مورد استفاده قرار میگیرد. AAS میتواند برای تعیین مقدار کمی بیش از ۷۰ نوع از عناصر مختلف مورد استفاده قرار گیرد. البته حد تشخیص برای همه ان ۷۰ عنصر مناسب نیست مثلا اگرچه اندازهگیری اورانیم در نرمافزار دستگاه جذب اتمی وارد شدهاست اما کمترین غلظتی که میتوان اندازهگیری کرد در حدود ppmاست که مقدار بزرگی است، لذا این روش دستگاهی را میتوان برای اندازهگیری حدود ۳۰عنصر با حد تشخیص مناسب (زیر ۱ ppm) بهکار برد. با توجه به قدمت دستگاه موجود در این آزمایشگاه هم اکنون 15 عنصر با اطمینان بالا مورد آنالیز قرار می گیرد.
در تجزیه جذب اتمی، ماده مورد اندازهگیری باید به حالت عنصری کاهش یابد، تبخیر شود و سر راه شعاع تابش منبع، قرارگیرد. در این فرایند نمونهها باید بهصورت محلول باشند. در اولین قدم آزمایش، محلول حاوی عنصر مورد نظر، بوسیله یک شعله که بهعنوان مثال با هوا و استلین میسوزد در دمای ۲۰۰۰ درجه سلسیوس (درجه حرارتی پایینتر از طیف تابشی) بخار میشود. در اثر بخار شدن، قسمت اعظم عناصر موجود در محلول به حالت خنثی در میآید و پرتوی تابش شده از لامپهای کاتدی (لامپ مخصوص برای هر عنصر) توسط اتمهای خنثی شده، جذب میشود. در این حالت شدت اشعه تابش اولیه کمتر میشود. تفاوت شدت دو پرتوی تابشی و خروجی معیار غلظت عناصر موجود در محلول است. عیب اصلی این تکنیک، وجود نیاز به یک لامپ منبع جداگانه برای هر عنصر مورد تجزیه است. برای رفع این نقیصه کوششهایی بهعمل آمده است تا یک منبع پیوسته بههمراه یک تکفامساز (تکفامساز جلوی منبع نور قرار میگیرد و طول موج مورد نظر را عبور میدهد) با قدرت جداکنندگی بسیار بالا بهکار گرفته شود. اما این تکنیک به اندازه بهکارگیری یک لامپ مخصوص برای هر عنصر رضایت بخش نیست.
اساس روش: اساس این تکنیک، استفاده از دستگاه جذب برای ارزیابی غلظت آنالیت در نمونه است، لذا نیازمند رابطهای بین میزان نور جذب شده توسط نمونه و غلظت نمونه هستیم که همان قانون بیر لامبرت است. بهطور خلاصه الکترونهای اتمها با جذب طول موج مشخصی (انرژی) میتوانند به سطوح بالاتر انرژی بروند و برای مدت کوتاهی به حالت برانگیخته در بیایند. میدانیم که این مقدار انرژی جذب شده برای هر اتم با اتم دیگر متفاوت است. به زبان دیگر هر عنصری فقط به یک طول موج مشخص پاسخ میدهد. باریک بودن پرتو نور در این روش موجب میشود تا انرژی خاصی تولید شود و این روش بسیار دقیق و انتخابپذیر باشد. هنگامی که اتم برانگیخته به حالت پایه برمیگردد طول موج مشخصی از خود ساطع میکند با اندازهگیری میزان جذب نمونه و رسم منحنی کالیبراسیون و قانون بیر لامبرت پی به میزان مجهول در نمونه میبریم.
2- تکفامسازها یا صافیها
یک دستگاه جذب اتمی باید قادر به تامین یک پهنای نوار به آن اندازه باریک باشد تا خط انتخاب شده برای اندازهگیری را از خطوط دیگری که ممکن است مزاحمت ایجاد کنند یا حساسیت تجزیه را کاهش دهند جدا سازد. آشکارسازها و شناساگرها برای تبدیل علامت انرژی تابشی به الکتریکی لولههای فوتو تکثیر کننده بهکار گرفته می شوند. دستگاه الکترونیکی قادر به تمییز دادن بین علامت مدوله شده از منبع و علامت پیوسته از شعله است.موارد کاربرد طیف بینی جذب اتمی وسیله حساسی برای تعیین بیش از 60 عنصر تامین میکند. عناصری مانند روی، آهن، نیکل، مولیبدن، وانادیم و غیره تا دقت چند میلیگرم در لیتر (ppm) قابل اندازهگیری با این دستگاه میباشند.
3- وسایل لازم برای تشکیل بخارهای اتمی
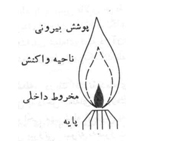
هدف از اتمسازی نمونه، تولید اتمهای آزاد است. اتمهای آزاد اتمهایی هستند که با اتمهای دیگر ترکیب نمیشوند. هیچ اتمی به حالت آزاد وجود ندارد بهجز اتم گازهای نادر که با هم به صورت مولکولی در میآیند. بنابراین برای ایجاد اتمهای آزاد ضروری است که مولکولها شکسته شوند. این فرآیند را اتمسازی گویند. بهترین روش برای اتمی کردن مولکولها، تفکیک آنها بهوسیله گرماست. برای آنالیز محلولها، از شعله به عنوان منبع گرما استفاده میشود و نمونه برای تبدیل به اتمهای آزاد در دمای زیاد گرم میشود. این روش را روش اتمسازی شعلهای میگویند. در روش غیرشعلهای کوره گرافیتی برای اتم سازی محلولها، محلولهای آبکی و نمونههای جامد مورد استفاده قرار میگیرد. دستگاه موجود در آزمایشگاه با روش شعلهای کار میکند.
4- دتکتور:
آشکارساز سیگنال مناسب با شدت نور دریافت شده تولیدکرده و در نهایت، جذب بهصورت عدد قرائت میشود.
دستگاه نمایش خروجی "
این قسمت، میتواند یک گالوانومتر، صفحه ثبات، اسیلسکوپ یا صفحه نمایشگرکامپیوتر با نرمافزارهای متنوع باشد.
نکات مهم در مورد ایمنی AAS:
محدودیتهای روش طیفسنجی جذب اتمی:
AAS توانایی تعیین یک عنصر را در هر لحظه دارد. اما این تکنیک به کندی صورت میگیرد و برای آنالیز چند عنصر روشی بسیار طولانی و خسته کننده است. تغییرپذیری در غلظت نمونه میتواند مشکلساز باشد، چون حدود دسترسی AAS بسیار محدود است.
نتیجهگیری:
درطیفسنجی جذب اتمی، عنصر مورد اندازهگیری باید به حالت اتمی کاهش یابد و سپس سر راه پرتو فرودی از منبع تابش مناسب قرار گیرد. با توجه به میزان جذب طیف عبوری از نمونه میتوان مقادیر عناصر فلزی و شبه فلزی در ترکیبات معدنی طبیعی و سنتزی، فلزات و آلیاژها را اندازهگیری نمود. از مزایای عمده طیفسنجی جذب اتم، ارزان بودن هزینه دستگاه و آنالیز است.
فرآیند انجام کار: